biogen
Biogen отчиталась лучше ожиданий и повысила прогноз на 2021 г.
- 22 октября 2021, 18:51
- |
Биотехнологическая компания Biogen (BIIB) отчиталась за 3 кв. 2021 г. (3q21) в среду, 20 октября. Выручка упала на 17,7% до $2,78 млрд, без изменений по отношению ко 2q21. Скорректированная чистая прибыль в расчёте на 1 акцию (Non-GAAP diluted EPS) составила $4,77 по сравнению с $5,64 за 3q20. Аналитики в среднем прогнозировали выручку $2,67 млрд и EPS $4,11. Чистая продуктовая выручка упала на 18% до $2,2 млрд. Продажи препарата Aduhelm от болезни Альцгеймера составили $300 тыс., тогда как аналитики ожидали $10,79 млн.
Обзор отчёта за 2q21 — см. по ссылке.
За 9 мес. 2021 г. выручка обвалилась на 22% до $8,25 млрд. Чистая продуктовая выручка упала на 20,7% и составила $6,65 млрд. Свободный денежный поток (FCF) $2,6 млрд против $4,3 млрд за 9 мес. 2020 г. Non-GAAP Diluted EPS $15,79 против $24,75 годом ранее. Денежные средства и эквиваленты и к/с фин.вложения $3 млрд. Долг $7,27 млрд, как и в конце 2q21. Показатель “Чистый долг / LTM EBITDA” ниже 2x.
Результаты по основным препаратам.
( Читать дальше )
- комментировать
- 329
- Комментарии ( 0 )
Biogen Inc. (биофрарм №1 в мире) - Прибыль 9 мес 2021г: $1,748 млрд (падение в 2,1 раза г/г)
- 20 октября 2021, 18:38
- |
Biogen Inc.
The number of shares of the issuer’s Common Stock, $0.0005 par value, outstanding as of July 21, 2021, was 149,033,443 shares.
www.sec.gov/ix?doc=/Archives/edgar/data/875045/000087504521000044/biib-20210630.htm
Капитализация на 20.10.2021г: $40,114 млрд
Общий долг на 31.12.2018г: $12,257 млрд
Общий долг на 31.12.2019г: $13,895 млрд
Общий долг на 31.12.2020г: $13,933 млрд
Общий долг на 30.06.2021г: $13,256 млрд
Общий долг на 30.09.2021г: $12,926 млрд
Выручка 2018г: $13,453 млрд
Выручка 9 мес 2019г: $10,707 млрд
Выручка 2019г: $14,378 млрд
Выручка 9 мес 2020г: $10,592 млрд
Выручка 2020г: $13,445 млрд
Выручка 1 кв 2021г: $2,694 млрд
Выручка 6 мес 2021г: $5,469 млрд
Выручка 9 мес 2021г: $8,248 млрд
Прибыль 9 мес 2018г: $3,529 млрд
Прибыль 2018г: $4,474 млрд
Прибыль 9 мес 2019г: $4,449 млрд
Прибыль 2019г: $5,889 млрд
Прибыль 9 мес 2020г: $3,703 млрд
Прибыль 2020г: $4,061 млрд
Прибыль 1 кв 2021г: $404,6 млн
Прибыль 6 мес 2021г: $1,430 млрд
Прибыль 9 мес 2021г: $1,748 млрд
investors.biogen.com/financials/sec-filings
Cambridge, Mass., October 20, 2021 — Biogen Inc. (Nasdaq: BIIB) сегодня опубликованы финансовые результаты за третий квартал 2021 года
( Читать дальше )
📉Акции Biogen рухнули на 8% из-за трудностей с лекарствами
- 09 сентября 2021, 19:38
- |
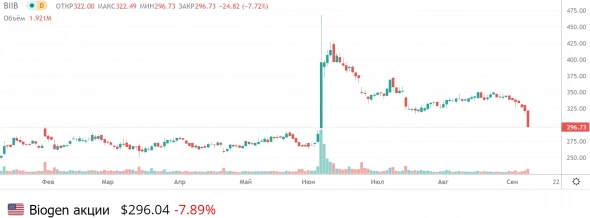
👉 Компания сталкивается с трудностями при выводе своего лекарство от болезни Альцгеймера на рынок. Об этом сообщил CEO компании
👉 Ранее в этом году FDA одобрило препарат от болезни Альцгеймера компании. Это вызвало раскол в врачебном сообществе США. В знак протеста три члена консультационной комиссии FDA уволились
👉 Проблемы с выходом на рынок могут быть связаны с высокой стоимостью препарата: $56 000
Biogen: первая выручка препарата от болезни Альцгеймера, споры продолжаются
- 15 августа 2021, 11:51
- |
Biogen Inc. (BIIB) отчиталась за 2 кв. 2021 г. (2Q21) 22/07. Выручка обвалилась на 24,6% и составила $2,78 млрд. Скорректированная прибыль в расчёте на 1 акцию (adjusted EPS) $5,68 против $9,85 за 2Q20. Аналитики в среднем прогнозировали выручку $2,61 млрд и adjusted EPS $4,55. Свободный денежный поток (FCF) $1,16 млрд против $1,84 млрд во 2Q20. Денежные средства и эквиваленты и к/с фин.вложения $3,05 млрд. Долг $7,27 млрд, как и в конце 1Q21. “Чистый долг / LTM EBITDA” менее 2x.
Результаты по основным препаратам.
Рассеянный склероз (multiple sclerosis)*. Выручка от продаж Tecfidera (dimethyl fumarate) обрушилась на 58,7% до $487,6 млн. В США продажи обвалились на 80% до $178,4 млн. Неутешительные результаты связаны с выходом дженериков на рынок США. В остальном мире выручка выросла на 15% до $309,2 млн. Доля Tecfidera 17,6% в выручке компании. Продажи Vumerity (diroximel fumarate) продолжили расти и достигли $90,9 млн по сравнению с $73,6 млн в 1Q21 и $8,7 млн во 2Q20.
Продажи Avonex (interferon beta-1a) упали на 20% и составили $310,9 млн. В основном из-за конкуренции с другими препаратами.
Выручка Tysabri (natalizumab) достигла $524,2 млн, что на 21,3% выше, чем во 2Q20.
( Читать дальше )
Eli Lilly подаст заявку в FDA по препарату от болезни Альцгеймера
- 29 июня 2021, 01:05
- |
Eli Lilly and Company (LLY) до конца года подаст заявку на ускоренную регистрацию препарата от болезни Альцгеймера. FDA одобрила ускоренное рассмотрение для кандидата donanemab, говорится в заявлении компании. Программа применяется к препаратам, данные клинических исследований (КИ) по которым свидетельствуют об очевидном улучшении состояния пациентов, и результаты существенно превосходят текущую одобренную терапию. Ранее по аналогичному пути компания Biogen получила одобрение FDA для препарата Aduhelm, но при условии, что будут предоставлены дополнительные доказательства его эффективности и безопасности. Решение FDA вызвало критику, т.к. панель независимых экспертов почти единогласно голосовала против одобрения.
Eli Lilly планирует подать заявку на одобрение кандидата donanemab, основываясь на результатах фазы 2 КИ, в которых приняли участие 272 пациента. Как и Aduhelm, donanemab нацелен на удаление белка бета амилоида (Аβ42 или N3pG) из клеток мозга, или так называемых амилоидных бляшек. В январе компания сообщила, что donanemab снижает у пациентов ухудшение состояния – сознания и функциональности. Замедление ухудшения состояния отмечено на 32% лучше в сравнении с плацебо по итогам 76 недель. Eli Lilly тем не менее отмечала, что статистически значимых результатов по достижениям целей второго уровня (secondary endpoints) пока нет. Некоторые аналитики не ожидали, что Eli Lilly подаст заявку до завершения фазы 3 КИ, включающей большее количество пациентов, результаты которого будут в 2022-2023 гг.
( Читать дальше )
Сектор здравоохранения "оздоровился" - Финам
- 25 июня 2021, 18:19
- |
Основной причиной, конечно, является то, что мировая экономика постепенно восстанавливается, эпидемиологическая ситуация нормализуется, а деловая и потребительская активность постепенно также возвращаются к нормальному уровню, пациенты возвращаются в поликлиники, в кабинеты врачей. Это положительно сказывается на довольно широкой когорте игроков рынка здравоохранения. И это привело к тому, что многие компании по итогам 2 квартала зафиксировали довольно неплохие результаты на фондовом рынке.
Отмечаем, что 2021 год может стать одним из рекордных за последние несколько лет по количеству лицензий, которые FDA выдала по новым препаратам и по препаратам по новым показаниям. Конечно, это связано с нормализацией эпидемиологической обстановки. Дело в том, что компании сейчас возвращаются к замороженным клиническим программам и исследованиям, которые были остановлены в 2020 году.
И мы хотели бы обратить внимание – и в стратегии мы это подчеркиваем – одно из ключевых событий для отрасли – одобрение от 7 июня 2021 препарата Aducanumab (адуканумаб) от компании Biogen, который стал первым за несколько десятилетий решением для пациентов с болезнью Альцгеймера.Ковалев Александр
ФГ «Финам»
За Какими Акциями я слежу Прямо Сейчас? / Интересные Акции / Intel, Adobe, Biogen, AirBnb, Palantir
- 21 июня 2021, 17:16
- |
2 трейдера: Biogen +38% / Падение Bitcoin / Apple – борьба за приватность пользователей
- 09 июня 2021, 14:54
- |
Акции Biogen выросли после одобрения лекарства от Альцгеймера - обзор
- 08 июня 2021, 14:46
- |
Акции Biogen выросли на 40% за день после одобрения американским регулятором FDA препарата адуканумаб от болезни Альцгеймера (будет продаваться под брендом Aduhelm). Какие перспективы для бизнеса компании открывают продажи лекарства?
Болезнь Альцгеймера в основном появляется у людей старше 65 лет, медленно разрушая память и навыки мышления. Полного понимания причин болезни нет. Особенностями являются накопление амилоидных бляшек и нейрофибриллярных клубков в тканях мозга.
В США от Альцгеймера страдает 5,8 млн человек, по всему миру количество заболевших оценивается более чем в 35 млн человек. Так как это болезнь пожилых людей, в будущем количество случаев будет расти из-за увеличения продолжительности жизни и среднего возраста населения. По прогнозам к 2050 году число заболевших превысит 100 млн человек.
До текущего момента в мире не было одобренных лекарств лечения болезни. Современные методы терапии лишь смягчают симптомы, не позволяя остановить или даже замедлить развитие заболевания. Предполагается, что препарат Biogen разрушает белок, формирующий в мозгу человека сгустки, которые вызывают проблемы с памятью и мышлением. Лекарство может стать первым в мире способом лечения, а не снятия симптомов Альцгеймера.
( Читать дальше )
- bitcoin
- brent
- cnyrub
- eurusd
- forex
- gbpusd
- imoex
- ipo
- nyse
- s&p500
- si
- usdrub
- акции
- алготрейдинг
- алроса
- анализ
- аналитика
- аэрофлот
- банки
- биржа
- биткоин
- брокеры
- валюта
- вдо
- волновая разметка
- волновой анализ
- вопрос
- втб
- газ
- газпром
- гмк норникель
- дивиденды
- доллар
- доллар рубль
- дональд трамп
- евро
- золото
- инвестиции
- инвестиции в недвижимость
- индекс мб
- инфляция
- инфляция в россии
- китай
- ключевая ставка цб рф
- кризис
- криптовалюта
- лукойл
- магнит
- мобильный пост
- мосбиржа
- московская биржа
- мтс
- натуральный газ
- нефть
- новатэк
- новости
- обзор рынка
- облигации
- опрос
- опционы
- отчеты мсфо
- офз
- оффтоп
- портфель инвестора
- прогноз
- прогноз по акциям
- путин
- раскрытие информации
- роснефть
- россия
- ртс
- рубль
- рынки
- рынок
- санкции
- сбер
- сбербанк
- сво
- северсталь
- смартлаб
- сущфакты
- сша
- технический анализ
- торговля
- торговые роботы
- торговые сигналы
- трейдинг
- украина
- финансы
- фондовый рынок
- форекс
- фрс сша
- фьючерс mix
- фьючерс ртс
- фьючерсы
- цб рф
- экономика
- экономика россии
- юмор
- яндекс


















 Новости тг-канал
Новости тг-канал

