Блог им. Koleso
Cтарение. Часть 3. Старение как изнашивание, как защита, как программа, как побочный эффект. Заключение. Кто виноват. Что делать.
- 24 июня 2020, 13:29
- |

Видеоконспект https://youtu.be/dsvNYHZCHqg Часть 2
Электронная книга t.me/kudaidem/1038
Часть 1 https://smart-lab.ru/blog/628950.php
Часть 2 https://smart-lab.ru/blog/629065.php
Часть III Я обвиняю
Попробую показать, как можно было бы решать задачу борьбы со старением, если бы мы только знали наверняка, кто в нем виноват.
Давайте представим себе живой организм в виде бочки, полной воды, то есть жизни. Каждая дощечка в бочке – это способ защититься от одного из врагов: свободных радикалов, опухолей, патогенных микробов. Жизнь может утекать через край бочки или поверх самой короткой из дощечек. Пусть какой-то из факторов в старении случайно оказался главным, например мутации в генах. Это означает, что дощечка, которая соответствует защите организма от мутаций, короче всех остальных.
единственная причина старения невозможна по техническим соображениям. все дощечки в бочке примерно одинаковой длины.
Расскажу об основных теориях старения и том, какие решения они предлагают для продления жизни. Для простоты рассказа они объединины в четыре группы:
одна рассматривает старение как неизбежность,
вторая – как защиту,
третья – как программу,
а четвертая – как побочный эффект молодости.
1. Виноват стресс: Старение как изнашивание
Первая группа теории старения, которая по-английски называется «wear and tear», то есть износ и распад. Это свободнорадикальная теория старения и причина распада тела кроется в повреждениях макромолекул. В них, в свою очередь, виноваты свободные радикалы, а своим появлением в клетках они обязаны страшному яду – кислороду.
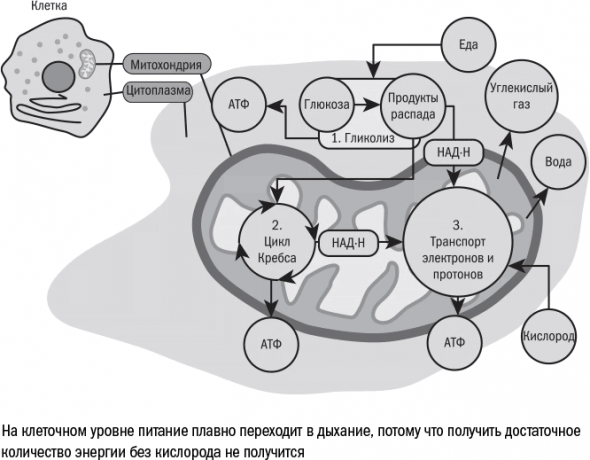
Поскольку первыми под удар активных форм кислорода попадают митохондрии, то одна из ветвей свободнорадикальной теории предполагает, что именно их повреждение движет старением. Ее так и называют – митохондриальная теория старения, – и именно ею занимался Обри ди Грей до того, как придумал свой «инженерный подход».
В ответ на сильный стресс клетки стареют, то есть перестают делиться, начинают выделять SASP (набор провоспалительных белков) и приобретают прочие признаки сенесцентности. Этот феномен назвали стресс-индуцированным старением (SIPS).
Одновременно с дыханием клетки производят антиоксиданты – вещества, которые нейтрализуют активные формы кислорода.
Логично предположить, что можно продлить жизнь, снизив уровень окислительного стресса. Вероятно, забравшись поглубже, голые землекопы скрылись не только от хищников, но и от источников окислительного стресса.
Лишаясь всей своей воды, личинки комара-звонца останавливают химические процессы в клетках. Высушенная личинка не ест и не дышит, не строит белков и не копирует ДНК, и на ее клетки не действует никакой стресс.
Некоторые авторы даже сравнивают беспозвоночных в состоянии ангидробиоза (высыхания) со Спящей красавицей из сказки, для которой время остановилось на сотню лет.
Но, останавливая старение, они останавливают и течение собственной жизни. Как говорил Лао-цзы, «овладение Поднебесной всегда осуществляется посредством недеяния. Кто действует, не в состоянии овладеть Поднебесной». Перефразируя его слова применительно к старению, можно сказать, что бессмертен только тот, кто не живет.
Отдельно стоит сказать пару слов о психологическом стрессе. Чем ниже психологический стресс, тем меньше стресс физиологический и тем активнее работает иммунная система.
Если стресс – неотъемлемое свойство жизни, то чем активнее организм живет, тем быстрее он должен стареть.
На основании этих умозаключений выдвинута теорию уровня жизни, или скорости жизни (the rate-of-living theory of aging). Ученые предположили, что у каждого организма есть свой запас энергии, «жизненной силы» (vitality), и чем быстрее он расходует ее, тем меньше живет. Так, повышая температуру окружающей среды дрозофил, удавалось сократить время их жизни.
Чем быстрее клетка расходует энергию, тем больше нужно ее произвести и, следовательно, тем больше образуется свободных радикалов.
Летучие мыши, рукокрылые освоили ряд секретов долголетия.
Чтобы удерживать свое, пусть и небольшое, тело в воздухе, летучие мыши непрерывно работают мышцами и расходуют энергию, часть из которой рассеивается в виде тепла. В результате температура тела у них почти все время держится на уровне более 40 °С, отсюда родилась концепция «полета как горячки».
летучие мыши научились тормозить свое воспаление, а их макрофаги – выделять больше противовоспалительных веществ. Одновременно с этим рукокрылые выработали устойчивость к вирусам, чтобы те не провоцировали иммунный ответ, и блокируют их размножение еще на ранних стадиях.
Таким образом, летучие мыши доказывают, что температура необязательно приближает смерть организма: всегда можно найти механизмы, которые позволят справиться с последствиями высокой скорости жизни.
У человека скорость обмена веществ с возрастом снижается.
жизненная сила – это запас сил на рост. Насколько быстро эта сила будет расходоваться, зависит от того, как организм распоряжается своими ресурсами, а это уже, в свою очередь, определяется фазой жизни. Чем реже периоды роста или медленнее сам рост – тем целее запас сил и тем дольше жизнь.
наша жизнь неразделимо связана с окислительным стрессом, и стресс же ее сокращает. Логично предположить, что, снизив уровень стресса в клетках, мы можем продлить собственную жизнь. Поэтому в конце ХХ века в моду вошли антиоксиданты, которые выступают в роли добрых сил в этой битве. Люди начали усиленно их поглощать, например, в составе чеснока, авокадо, бобов, ягод и темного шоколада или пищевых добавок. Появились так называемые зеленые коктейли и косметика с антиоксидантами – все они были призваны снизить окислительный стресс в клетках и продлить молодость.
А российский академик Владимир Скулачев, сторонник митохондриальной теории старения, придумал свой антиоксидант (наподобие витаминов С и Е) на все случаи жизни: ион SkQ («ион Скулачева»), который должен был смягчать окислительный стресс в митохондриях и беречь их смолоду.
Но в большинстве экспериментов на здоровых объектах от такого лечения больше вреда, чем пользы.
соображение, которое могло бы объяснить провал антиоксидантов как средства для продления жизни, заключается в том, что клетка регулирует производство собственных антиоксидантов в зависимости от количества активных форм кислорода. Если в какой-то момент их становится слишком мало, выработка антиоксидантов прекращается и клетка остается беззащитной. Теперь в случае настоящего стресса ей будет нечего противопоставить свободным радикалам. И судя по тому, что мы сегодня знаем об антиоксидантах, они могут быть действительно эффективны в больном организме, в условиях хронического воспаления, но едва ли чем-то помогут здоровым людям.
явление – стимулирующее влияние малых доз стресса – называют гормезисом, а сами стрессовые факторы – горметинами. Гормезис работает примерно так, как мы представляем себе закаливание. Сама по себе зарядка не приносит человеку большой пользы, но держит в тонусе мышцы, чтобы можно было в любой момент убежать от опасности. Горметины вызывают легкий стресс, который запускает в клетке работу защитных механизмов и не дает им отключиться.
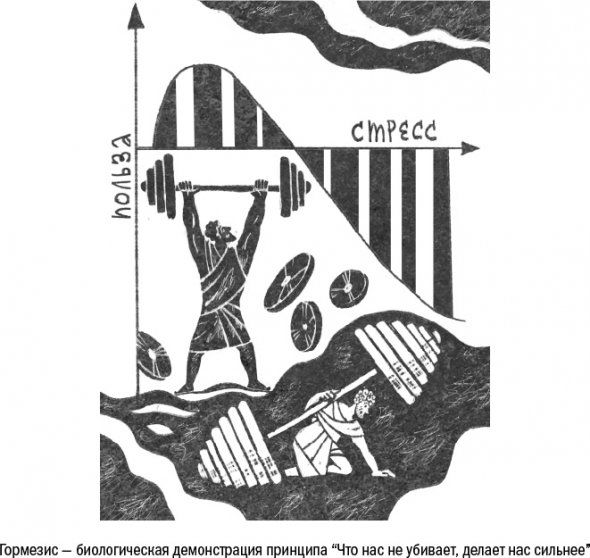
Фактически горметины – это те же самые факторы, которые в больших количествах сокращают жизнь: перепады температуры, радиация, тяжелые металлы, окислители, спирты, повышенная гравитация, голодание. В этот же список попадают растительные алкалоиды, экстракты чая, темного шоколада и шпината. Вопрос в дозе: силе и длительности действия. Большие дозы вызывают гибель клетки, дозы поменьше – стресс-индуцированное старение, маленькие дозы – деление и снижение ущерба от окислительного стресса, то есть гормезис.
Например, есть данные о том, что низкие дозы мышьяка улучшают репарацию у пожилых людей, а ботулотоксина – притупляют боль и расслабляют мышцы. Работники ядерных электростанций реже умирают от рака. Голодание запускает работу шаперонов, а слабый психический стресс – который у людей вызывают среди прочего решение задач и медитация – улучшает работу иммунной системы, по крайней мере у мышей.
эти безумные эксперименты лишь подтверждают общее правило: немного стресса – полезно.
Продолжительность жизни организма действительно в существенной степени определяется стрессом, а точнее, соотношением сил, которые производят и нейтрализуют активные формы кислорода.
Вадим Гладышев предложил похоронить свободнорадикальную теорию старения и заменить ее на общую теорию ущерба (damage theory), который складывается из всех процессов, повреждающих клеточные макромолекулы.
Остается только закаливать клетки изнутри, привыкая к стрессу
2. Виноват рак: Старение как защита
Раковая и сенесцентная клетки в чем-то довольно сильно похожи друг на друга. Обе они в некотором роде маргиналы и преследуют свои интересы, не обращая внимания на соседей.
Но, раковая клетка для старой – скорее, зловещая тень, напоминание о том, что будет, если вовремя не остановиться.
Рак неплохо вписывается в портрет возрастной болезни. В его основе лежит сдвиг равновесия между делением и гибелью клеток: первое начинает доминировать над вторым. Опухолевые клетки делятся, соседние – гибнут, не выдержав конкуренции, и освобождают место в ткани для роста – возникает тот самый замкнутый круг, который усиливает любое возрастное заболевание.
Некоторые исследователи возлагают вину за развитие рака на его окружение: дело не в клетках, которые ломаются, а в их соседях, которые позволяют им выжить.
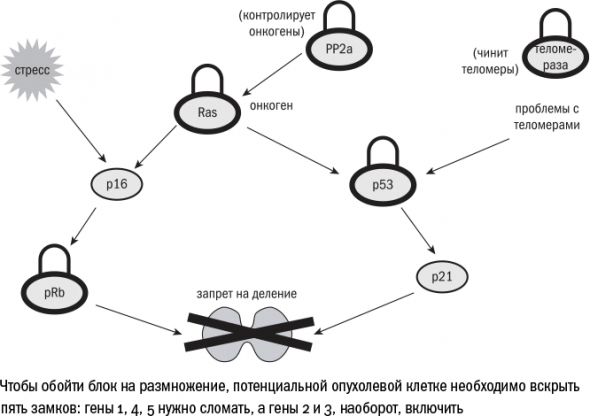
Опухолевая клетка нарушает пять главных принципов, которых придерживаются клетки в ткани:
1. Контроль рождаемости.
2. Кодекс чести. Законопослушная клетка осознанно умирает, как только становится опасна для общества. Опухолевая клетка держится за свою жизнь до конца.
3. Разделение труда. При опухолевой трансформации клетки теряют свою специализацию, дедифференцируются и разрывают контракт с обществом, пренебрегая своими обязанностями и игнорируя запреты.
4. Распределение благ. Опухолевые клетки переходят на быстрый и малоэффективный гликолиз (это называют эффектом Варбурга) и создают так называемую ловушку: бездонную яму, в которую утекает глюкоза, оставляя ни в чем не повинных соседей голодными.
5. Общественные пространства. Для клеток опухоли внеклеточное вещество – главный барьер на пути к расселению и захвату новых территорий, поэтому они всеми способами пытаются его расщепить (и сенесцентные клетки им в этом помогают).
Старениене вызывает раксамо по себе, а оба они независимо происходят из одной общей причины – накопления мутаций.
Парадокс – отсутствие связи между размерами тела, продолжительностью жизни и частотой заболевания – называют парадоксом Пето.
Разные животные придерживаются разных стратегий противоопухолевой защиты.
Первая стратегия для маленьких короткоживущих зверей – непротивление раку.
Вторая стратегия — остановить размножение подозрительных клеток на начальных этапах, не давая им шансов проверить, вырастут они в опухоль или нет.
Крупные же млекопитающие, начиная с бобров и заканчивая слонами и китами, следуют третьим путем и делают ставки на поздние механизмы защиты — ограничение деления и потеря теломер.
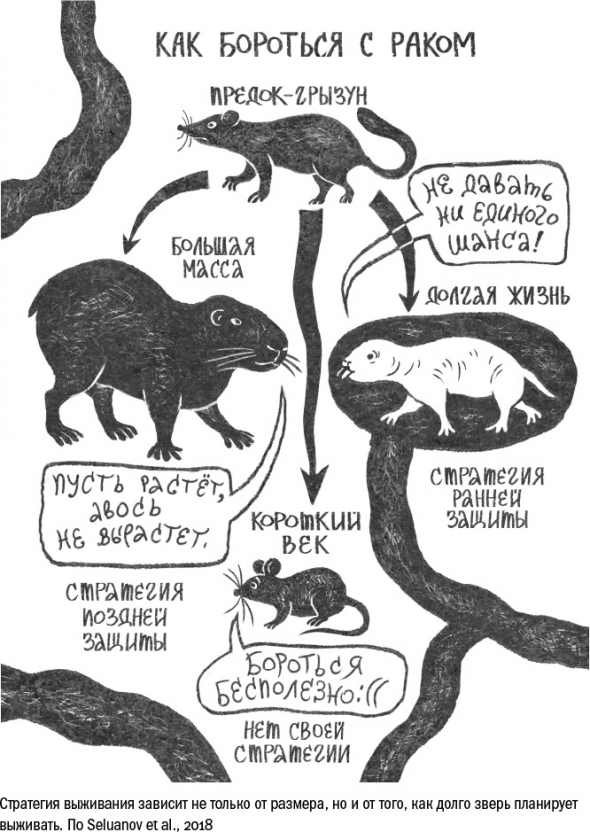
Разделение стратегий противоопухолевой защиты на три типа – сдаваться, стрелять на опережение или добить выживших – на самом деле довольно условно.
Человек, несомненно, относится к третьей группе.
если мы однажды и сможем позаимствовать что-то у голых землекопов, то это будет именно способ остановить развитие рака в зародыше.
Под действием стрессовых факторов белок р53 становится активным.
Если стресс продолжается, то «просыпается» еще один белок-супрессор – р16. Он мешает работе белков, запускающих деление клетки, и под его действием остановка клеточного цикла становится необратимой. Именно поэтому его используют как маркер сенесцентных клеток. Наконец, р16 активирует последний белок-супрессор – Rb, который занимается переупаковкой ДНК в ядре.
После того как он наводит порядок в ядре, потенциальные онкогены оказываются убраны «поглубже», то есть свернуты поплотнее, и больше себя не проявляют. Зато в открытом доступе оказываются гены SASP. Так клетка становится сенесцентной.
Два возможных пути старения – через р53 (стресс-индуцированное) или через Rb (онкоген-индуцированное) – становятся ответом на разные стимулы.
По части поздней защиты землекопу у нас работает система укорачивающихся теломер.
В половых клетках работает фермент, способный копировать ДНК без потери теломер. Это теломераза — она не копирует всю хромосому целиком, а занимается только восстановлением концов.
теоретически ничто не мешает клетке, в которой работает теломераза, жить вечно.
Теломеразу постоянно производят лишь половые клетки и, в меньшем количестве, стволовые. Остальные же никак не могут сохранить свои теломеры целыми.
Все три типа старения – стресс-индуцированное, онкоген- индуцированное и репликативное – сходятся к одним и тем же сигнальным клеточным путям.
Более того, эти три механизма тесно переплетены друг с другом
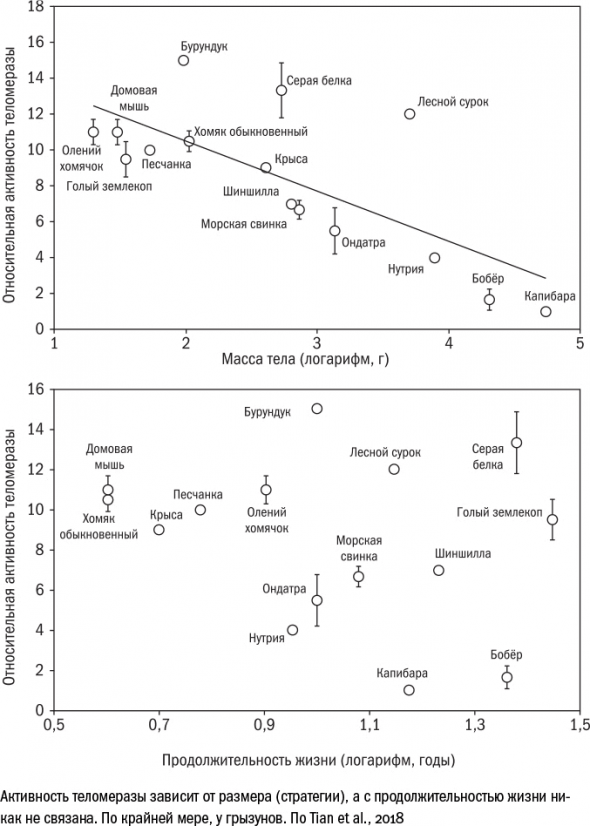
Никакой связи между вечной жизнью и работой теломеразы нет: что у мыши, что у землекопа она активна в одинаковой степени, а продолжительность жизни различается в десяток раз.
Тем не менее можно представить себе, что удлинение теломер могло бы продлить жизнь если не целого организма, то отдельных его клеток. Известно, например, что если ввести дополнительный ген теломеразы в клетки, где собственный ген выключен, то клетка или целая мышь начинают жить дольше.
Людям ген теломеразы пока никто не вводил – за одним исключением. В 2015 году американка Элизабет Перриш показательно сделала себе инъекцию обезвреженного вируса, который «заражает» клетки теломеразой. На момент инъекции телемеры были длиной в 6700 нуклеотидов, через год после – уже 7330, и через два года – 8120. Перриш называет это омоложением на 20 лет. Но учитывая, что предел, после которого клетка становится сенесцентной, лежит в районе 2000 нуклеотидов, средняя длина у человека – 7000, а стандартная погрешность измерений – около 700, сложно назвать эти результаты революционными. Все данные, которые приводит Перриш, попадают в пределы нормы, а о том, что именно вызвало изменение длины ее теломер (и вызвало ли), остается только гадать.
Можно подойти к проблеме и с другого конца: подействовать на клетку веществом, которое активировало бы работу теломеразы. Сегодня мы знаем одно такое вещество –ТА-65, выделенное из корней астрагала перепончатого.
ТА-65 снизил у людей проявления сердечно-сосудистых заболеваний и помог приостановить возрастную потерю зрения.
Попробуем разобраться, в каких отношениях на самом деле находятся старение и рак. С одной стороны, рак вызывает старение, устраивая клеткам стресс: выделяет токсины, отбирает у них еду, разрушает межклеточное вещество. Старость, в свою очередь, вызывает рак: сенесцентные клетки выделяют SASP и ослабляют защиту организма. Возникает замкнутый круг, как и во многих других возрастных болезнях.
С другой стороны, старость служит защитой от рака: именно для этого подозрительные клетки превращаются в сенесцентные на ранних стадиях под действием стресса или онкогенов или на поздних – через укорочение теломер.
Действительно, распространенность злокачественных опухолей падает после какого-то возрастного порога.
Возможно, все, кто мог пострадать от рака, уже погибли к 100 годам, а в живых остались только самые стойкие. Как говорилось в пьесе Леонида Филатова, J «но какие выживают – те до старости живут».
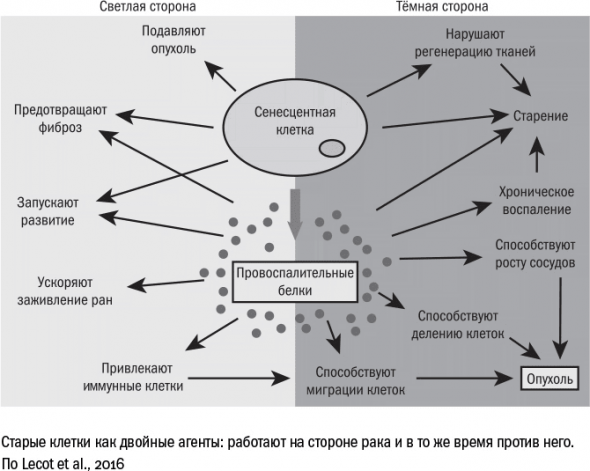
Между старением и раком организм выбирает меньшее из двух зол, то, которое позволит ему дольше прожить в сложившихся условиях.
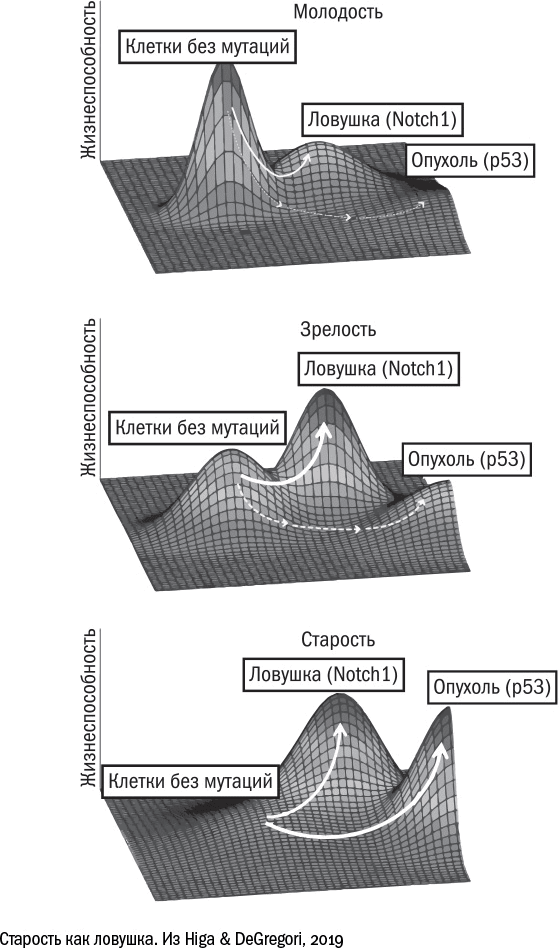
Победив рак, мы столкнемся лицом к лицу с проблемой сенесцентных клеток. Избавившись от старения, мы останемся наедине с нерешенной проблемой рака.
заполучить одновременно и долгую жизнь, и низкий риск развития рака, кажется, пока невозможно.
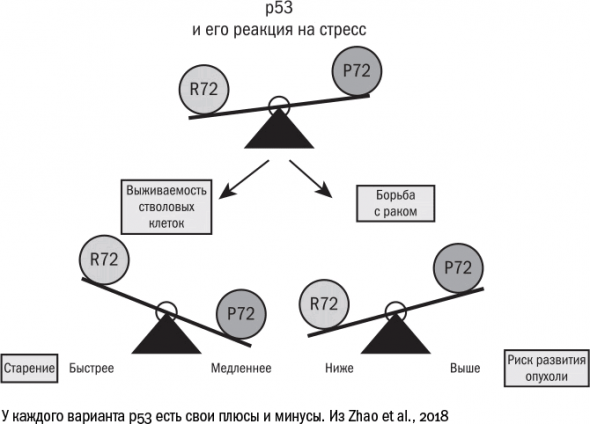
Сенолитики – лекарство, которое уничтожают только старые клетки.
Модельные мыши INK-ATTAC под действием сенолитика прожили в среднем на треть больше контрольных животных. Оказалось, что сенолитик борется с возрастными болезнями.
Подавляющее большинство известных на настоящий момент сенолитиков – это противоопухолевые лекарства, только применяются они в небольших дозировках.
Первыми найденными сенолитиками стали вещества дазатиниб и кверцетин.
Дазатиниб блокирует пути передачи сигнала, которые способствуют выживанию опухоли, и хорошо себя показал против сенесцентных клеток жировой ткани.
Кверцетин, вещество растительного происхождения, блокирует другие сигнальные пути и лучше справляется со старыми клетками в красном костном мозге и стенке сосудов. Вместе они воспроизводят эффекты модели INK-ATTAC, спасая мышей от фиброза легких, ожирения печени, остеопороза и последствий облучения.
Дазатиниб и кверцетин стали первыми сенолитиками, которые вышли на стадию клинических испытаний на людях. Их действие проверили у пожилых людей с фиброзом легких. В результате улучшилось общее самочувствие пациентов, они стали быстрее и дольше ходить.
Но, говоря о сенолитиках, важно помнить, что сенесцентные клетки – не абсолютное зло. Они необходимы для перестройки тканей. Например, по некоторым данным, убийство сенесцентных клеток в поджелудочной железе может привести к диабету.
3. Виноваты гены: Старение как программа
Существуют теории запрограммированного старения.
Они самые оптимистичные: ведь если во всех наших бедах виновата одна-единственная программа, то ее можно выключить, и старение выключится вместе с ней. Проблема только в том, что мы все еще не знаем, существует ли она на самом деле.
Геронтологи развивают эволюционную теория старения, находя все новые и новые плюсы для организмов в программе старения и смерти.
Программу смерти они считают логичным продолжением программы развития организма.
Непосредственно механизм запрограммированного старения предложил в 1997 году Владимир Скулачев, специалист в области клеточного дыхания и один из создателей биоэнергетики, научной дисциплины, которая занимается обменом энергии в клетке.
Скулачев обратил внимание на то, что у одноклеточных организмов – в частности, дрожжей – тоже встречается запрограммированная смерть, а механизмы ее схожи с апоптозом, клеточным самоубийством в организме млекопитающих. В обоих процессах участвуют белок р53, а также антиоксиданты и шапероны (белки – упаковщики белков).
Поэтому Скулачев предложил считать гибель одноклеточных дрожжей и гибель отдельных клеток в многоклеточных организмах единым явлением и назвал его феноптозом.
Когда феноптоз запущен, механизмы ремонта выключаются и начинают накапливаться те самые повреждения, которые приводят в конечном счете к старению или апоптозу клеток, а затем и к смерти организма.
Скулачев считает старение и рак следствиями одной программы и называет рак быстрым феноптозом, а старение – медленным, постепенным.
Программа старения и смерти, по Скулачеву, – это проявление альтруизма. Слабые организмы уступают место своим сильным собратьям.
Пример, тихоокеанский лосось умирает сразу после того, как размножился, и тем самым, вероятно, освобождает место для развития своих потомков, а своим телом подкармливает беспозвоночных, которые тоже впоследствии станут пищей для следующего поколения.
Что характерно, ни землекопы, ни летучие мыши, ни другие животные, которых относят к пренебрежимо стареющим, практически не болеют раком – и это подтверждает идею Скулачева о том, что рак и старение – явления одного рода.
Наконец, если программа существует, то ее можно выключить искусственно. Например, самцы австралийской бурой сумчатой мыши, как и лососи, погибают вскоре после спаривания. Оказалось, что для того, чтобы вызвать у них скорую смерть, достаточно феромонов самки, а если кастрировать или изолировать самцов, то можно продлить им жизнь до уровня самок. Того же эффекта можно достичь и посредством манипуляций с генами: выключения одного-единственного гена бывает достаточно, чтобы продлить жизнь дрозофилы в 4–10 раз.
С позвоночными, правда, такого эффекта достичь не удается – даже мыши, на которых уже перепробовали все, пока дольше четырех лет не живут.
Сторонники теории запрограммированного старения не теряют надежды и продолжают поиски программы в наших генах.
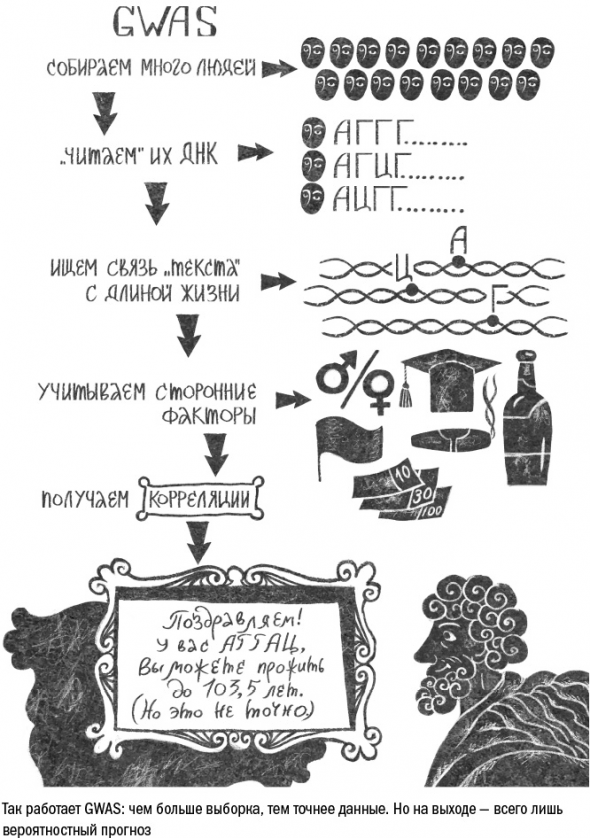
Они рассчитывать на то, что на земном шаре естественным путем уже скопилось достаточно разных генетических комбинаций, чтобы найти среди них какую-нибудь закономерность.
Основной метод, который для этого используют сейчас, – это полногеномный поиск ассоциаций (genome-wide association studies, GWAS).
Ученые собирают последовательность геномов разных людей, а затем ищут связь между продолжительностью их жизни и отличиями в последовательности отдельных генов. Иными словами, пытаются построить модель, которая позволила бы предсказать срок жизни человека на основе тех вариантов генов, которые он несет в своих клетках.
Для этого нужна большая выборка – в тысячи, а лучше сотни тысяч людей. За ней ученые обычно обращаются в биобанки – это базы данных, которые составлены по результатам многолетних исследований.
Таких исследований уже было немало, и на их основе можно сделать два важных вывода. Первый – оптимистичный: долголетие определенно наследуется.
У потомков долгожителей, например, на 62 % ниже риск смерти от всех причин, чем у контрольной группы того же года рождения, на 71 % ниже риск смерти от опухолей и на 85 % – от болезней сердца.
Но есть и пессимистичный вывод: единого «гена долголетия» или даже группы таких генов, судя по всему, не существует.
Сейчас принято говорить не о зависимостях, а о корреляциях, то есть статистических связях долголетия с теми или иными вариантами генов.
И когда мы видим сообщение о том, что вариант номер 25 гена А коррелирует с долгой жизнью, не стоит радоваться раньше времени. Из этого факта, например, не следует, что если человек исправит ген А в своих клетках на нужный вариант (а это рано или поздно станет возможным), то обязательно проживет дольше, чем мог бы со своим исходным вариантом гена. Корреляция – это не причинно-следственная связь, а некоторая статистическая закономерность, которую еще предстоит объяснить.
Например, может оказаться, что вариант номер 25 гена А распространен у потомков какой-нибудь знатной семьи, которые традиционно богаты и следят за своим здоровьем и поэтому живут дольше, – а любому другому человеку этот вариант гена никакой пользы не принесет.
Так как же правильно ответить на вопрос, зависит продолжительность жизни от генов или нет? Для этого ученые пользуются понятием наследуемости. Это вклад генетического разнообразия в разнообразие продолжительности жизни.
Считается, что наследуемость долголетия – 15–30 %.
Среди долгожителей женщин обычно больше в несколько раз, но болеют они сильнее и чаще мужчин, даже те, кто преодолели рубеж 90 лет. Это парадокс смертности-уязвимости.
Первая важная особенность женщин заключается в работе иммунной системы. По некоторым данным, тестостерон сильнее подавляет активность иммунитета, чем женские половые гормоны. У молодого организма это снижает риск развития аутоиммунных заболеваний, но в старости, когда воспаление помогает очищать организм от старых клеток, женщины оказываются в выигрыше.
Второе преимущество женщин перед мужчинами – в спасительном действии эстрогенов на клетки в тканях. Они не только стимулируют рост и деление клеток, но и защищают их от активных форм кислорода.
Продолжительность жизни самцов сокращают и гены, и гормоны, но гены (точнее, Y-хромосома) – сильнее.
Можно предположить, что самая выигрышная стратегия для долгой жизни – избежать наиболее распространенных болезней. Но если это так, то набор генов, связанных с долголетием, будет меняться по мере развития медицины.
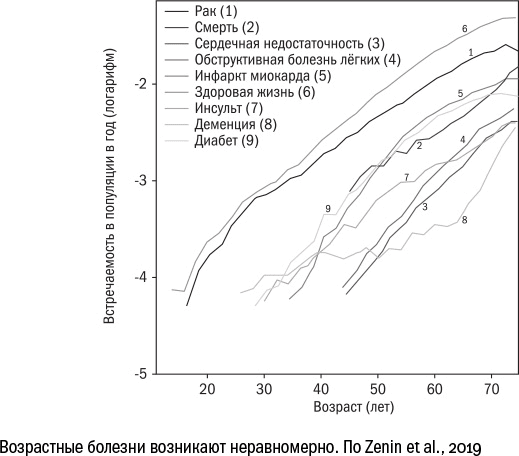
В 2006 году японские ученый Яманака придумал способ репрограммировать клетки, то есть возвращать их из дифференцированного состояния обратно в стволовое.
Для борьбы со старением было бы удобнее научиться репрограммировать клетки in vivo, то есть внутри живого организма. Постепенно оказалось, что для этого есть все предпосылки: репрограммированию поддаются любые клетки человека, в том числе сенесцентные клетки и клетки, взятые у долгожителей. После обработки факторами Яманаки к этим клеткам возвращается молодость – и по длине теломер, и по набору работающих генов, и по часам метилирования они начинают напоминать клетки зародыша.
Но если омолаживать клетки непрерывно, то взрослые клетки будут превращаться в эмбриональные и образовывать опухоли. Именно это произошло с мышами, у которых ученые усилили экспрессию факторов Яманаки.
Чтобы омоложение не заканчивалось ростом опухолей, нужно как-то научиться дозировать работу факторов Яманаки.
История с репрограммированием целого организма находится еще только в начале своего пути.
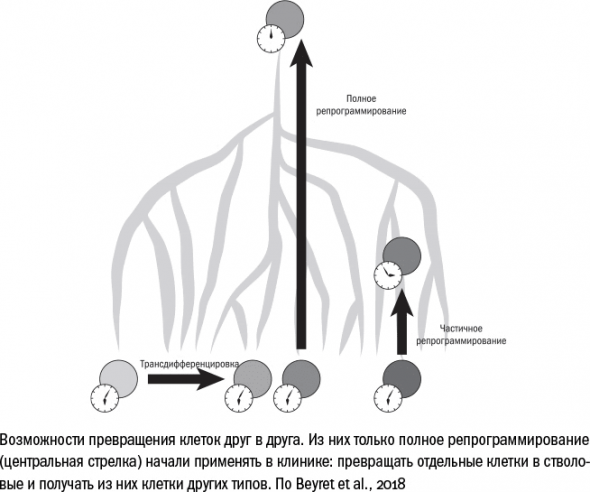
Кстати, клетки голого землекопа, в отличие от клеток мыши или человека, к репрограммированию устойчивы. Вероятно, это еще одно следствие механизмов, с помощью которых голый землекоп защищается от рака. Но, так или иначе, это лишает нас возможности попробовать продлить его жизнь еще больше. Получается своеобразный парадокс: животное, которое служит опорой теории запрограммированного старения, не способно обратить вспять единственную программу – развития и дифференцировки, – существование которой убедительно доказано.
4. Виновата молодость: Старение как побочный эффект
В последней части рассказа продвину идеи: ждать, поститься, размышлять и знать меру.
Ресурсы онанизма ограничены, а износ неизбежен, и возникает старость – побочный эффект, неприятное следствие программы вечной молодости. В таком случае лучшее, что мы можем ей противопоставить, – терпение, ожидание, смирение и замедление развития.
По теории накопления мутаций: старение вызвано накоплением губительных мутаций, которые не отсеивает естественный отбор, поскольку проявляются они только после определенного возраста.
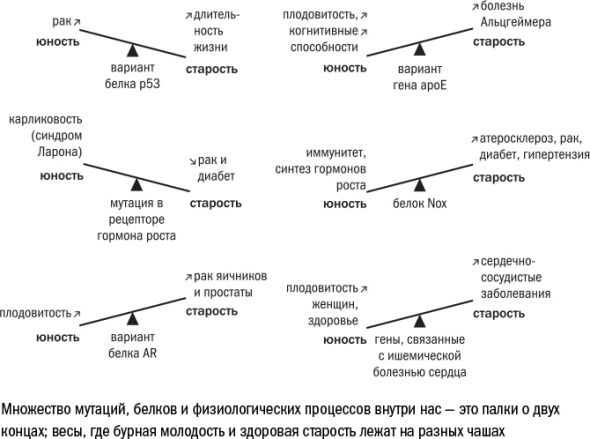
Чаще всего губительные мутации «покупают» себе место в геноме, повышая шансы молодых особей на размножение.
С точки зрения геронтологов отбор недальновиден: отбирая то, что приносит пользу здесь и сейчас, он «не задумывается» о последствиях, и за его поспешные решения нам всем предстоит расплачиваться в старости.
Но, если старение вызвано накоплением конкретных вредоносных мутаций, то что мешает назвать его генетической болезнью и относиться к нему соответственно?
Ведь, вскоре, мы научимся чинить гены и заменять их на более благоприятные для долгой жизни варианты.
Если теория антагонистической плейотропии верна, то это значит, что в старом организме протекают те же процессы, что и в молодом. В таком случае старение можно рассматривать как непосредственное и излишнее продолжение развития.
А старение можно сравнить с хождением вслепую: "…чем дольше вы блуждаете с закрытыми глазами, тем сильнее отклоняетесь от намеченной траектории".
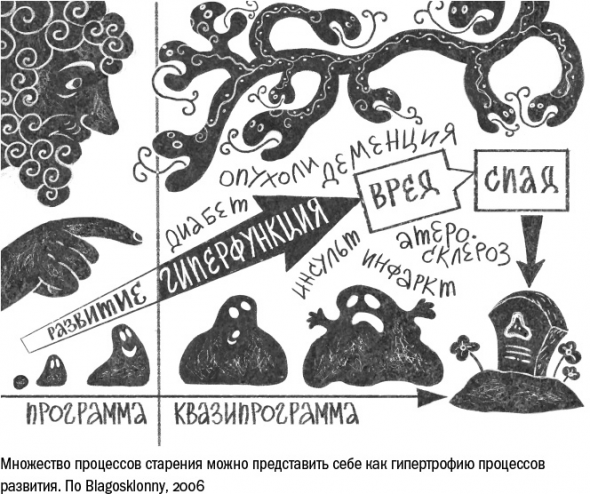
Старость, по американскому герантологу Благосклонному, предстает в виде гиперфункции, гипертрофированного проявления программы развития.
Например, старческая гипертония – это итог непрерывного повышения давления. Но, будучи один раз запущена, программа не выключается, – и давление продолжает расти, пока не превращается в гипертонию, типичное возрастное состояние.
То же происходит и со зрением: пока ребенок маленький, ему важно рассматривать близко расположенные объекты. С возрастом для человека становятся важны и более далекие объекты, поэтому хрусталик (линза, которая преломляет свет в глазу) растет и становится жестче и минимальное фокусное расстояние достигает 16 см в 40 лет, а к 60 может дойти до 100 см. Так развивается дальнозоркость, которую часто можно встретить у пожилых людей.
Чрезмерное свертывание крови вызывает тромбоз, избыточное воспаление – аутоиммунные реакции, неумеренное накопление жирных кислот – ожирение. Все это Благосклонный считает следствием того, что у программы развития нет естественного выключателя.
Старение клеток, согласно теории Михаила Благосклонного, тоже вызвано гиперфункцией, а точнее – гиперстимуляцией.
В некотором смысле клетка повторяет судьбу организма в целом: чем быстрее она растет и размножается, тем меньше она живет.
Глубинный механизм роста, тот самый главный рубильник, который включает квазипрограмму старения на клеточном уровне, давно известен: его имя TOR – это аббревиатура: Target Of Rapamycin, то есть «мишень действия рапамицина».
В клетках млекопитающих TOR входит в состав двух комплексов с другими белками, для простоты будем называть их общим именем mTOR.
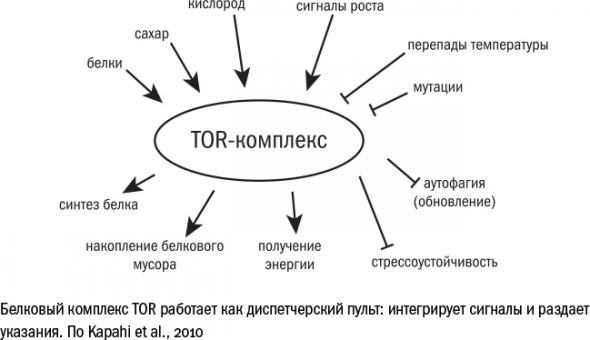
Комплекс mTOR служит в некотором роде центром принятия клеточных решений. Основные два его информанта – это факторы роста (снаружи) и питательные вещества (изнутри).
Важная нить, которая связывает сигнальный путь TOR с долголетием – биологические ритмы, наш внутриклеточный аналог дня и ночи.
Суточные ритмы не ограничиваются регуляцией сна и бодрствования, а влияют на бóльшую часть клеточной жизни. В течение дня ритмично колеблется работа примерно половины генов в клетках млекопитающих.
В клеточная ночь: перестают работать «дневные» гены, на смену им приходят «ночные».
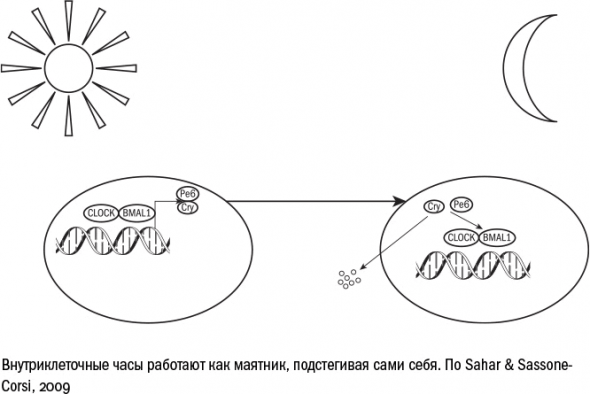
Внутриклеточные часы по всему организму нужно время от времени сверять, чтобы они продолжали идти в такт. За это отвечает гормон мелатонин, который производится в головном мозге. Важную роль играет и ежедневная активность человека. Если в организм поступает пища – значит, настал день. Если сигналы для роста и обмена веществ притихли – время спать. И здесь, конечно, на сцене снова оказывается TOR: почувствовав присутствие еды, он отдаляет наступление клеточного дня: зачем заканчивать эти сутки, если еды еще достаточно?
Сбой биоритмов связывают с самыми разными заболеваниями – от ожирения и сердечно-сосудистых болезней до рака. Эти опасности могут подстерегать не только любителей есть по ночам, но также людей, работающих в ночную смену.
Есть даже подозрение, что из-за электрификации полярных регионов выросла заболеваемость раком у жителей Арктики.
Вероятно, это повод уделять больше внимания своим биоритмам: не стимулировать клетки лишний раз, не будить TOR и не устраивать клеткам день посреди ночи.
Первые данные о том, как ограничение в еде влияет на продолжительность жизни, появились из бытовых наблюдений. После Первой мировой войны подсчитали, что смертность в Копенгагене сократилась на 34 % – и связал это с тем, что жители столицы были вынуждены меньше есть.
Похожая история развернулась в Норвегии уже во время Второй мировой войны: еды не хватало, а количество смертей от сердечно-сосудистых заболеваний упало на 30 % по сравнению с довоенным временем.
Третий эксперимент невольно поставили над собой жители Окинавы: продолжительность жизни на острове была выше, чем в среднем по Японии, а долгожители встречались в четыре-пять раз чаще. Исследователи связывают это с тем, что традиционный рацион окинавцев – овощи, фрукты, рыба, соя и рис – содержит меньше калорий, чем рацион жителей других регионов Японии.
Недокормленные крысы жили дольше.
В большинстве случаев ограниченные в еде существа все-таки жили дольше тех, кто ел вволю.
Так или иначе, сегодня ограничение калорий (calorie restriction) считается самым эффективным негенетическим методом продления жизни. Оно стало золотым стандартом «омоложения»: если появляется, например, новый маркер биологического возраста, то он должен отражать не только старение организма со временем, но и «омоложение» в результате голодания.
В отсутствие энергии клетка накапливает меньше побочных продуктов обмена и медленнее изнашивается (аргумент из области теории ущерба и накопления молекулярного мусора). В то же время дефицит еды вызывает в клетке легкий окислительный стресс – и действует как горметин, запуская работу антиоксидантов и систем репарации (подкрепляя свободнорадикальную теорию старения).
Наконец, в отсутствие еды не работают гиперстимуляторы клетки – инсулин, инсулиноподобный фактор роста и TOR. Поэтому клетка включает аутофагию – переваривание белков и органелл, – чтобы добыть себе строительные материалы, и сдвигает баланс «размножение – поддержание» в сторону последнего, то есть репарации ДНК и ремонта других клеточных макромолекул.
При голодании снижаются концентрации гормона роста, инсулина и ИФР в плазме крови и возрастает количество стресс-гормонов надпочечников. Вместе эти события приглушают воспаление в организме, что может быть полезно для лечения разных болезней вне зависимости от продления жизни. Кроме того, голодание оставляет клетки без глюкозы, что сильнее всего бьет по раковым и сенесцентным клеткам.
В отсутствие глюкозы стареющие клетки перестают выделять провоспалительные белки, а раковые клетки гибнут. Именно поэтому голодание иногда назначают после операций и при лечении опухолей.
Эксперимент «Биосфера 2», в ходе которого испытуемые провели два года в замкнутой экосистеме. Первые полгода они ели всего по 1784 килокалории в день, а оставшиеся полтора года – по 2000. Их состояние здоровья (количество жира, давление, состав крови, концентрация гормонов) улучшилось к моменту окончания эксперимента, однако, для них нет контрольной группы, и их не с кем сравнить.
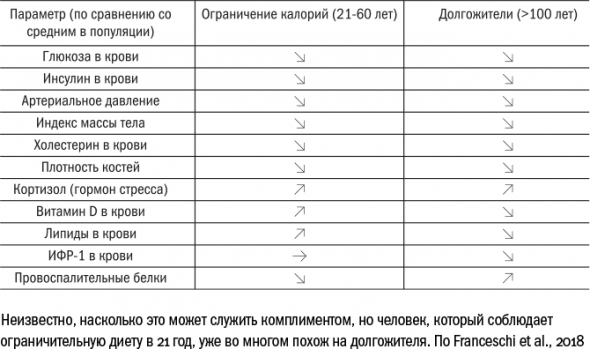
Испытание, которое сейчас снабжает ученых тщательно выверенными данными, – американский проект CALERIE (Comprehensive Assessment of Long-term Effects of Reducing Intake of Energy – полная оценка долгосрочных эффектов от снижения потребления энергии).
Это исследование идет всего несколько лет, а его участники – молодые люди в возрасте от 21 до 51 года, поэтому делать выводы о продлении жизни, безусловно, слишком рано. По разным физиологическим параметрам – обмену веществ, массе тела, давлению крови и так далее – люди, которых ограничивают в калориях, напоминают долгожителей.
В научном сообществе нет до сих пор согласия по поводу того, как именно стоит себя ограничивать в еде.
У людей необходимое количество калорий рассчитывают исходя из ежедневных энергозатрат: насыщение – это состояние, когда человек получает столько же энергии, сколько тратит.
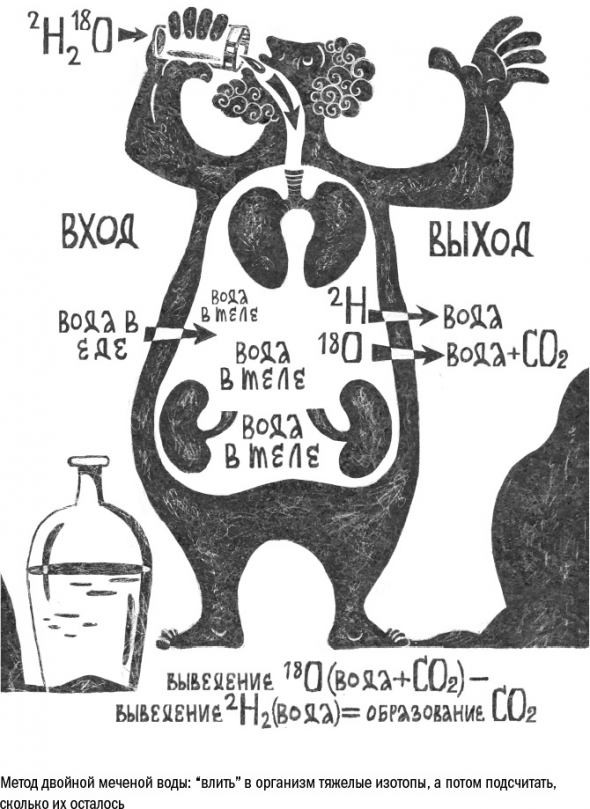
Есть несколько способов измерить энергозатраты. Самый простой – подсчитать количество выдыхаемого углекислого газа.
В экспериментах с людьми – например, в проекте CALERIE – используют более удобный метод с участием двойной меченой воды. Это вода, в состав которой входят тяжелые изотопы кислорода и водорода, то есть атомы с лишним нейтроном в ядре. Для здоровья она совершенно безвредна. Испытуемым дают выпить меченую воду, а затем подсчитывают количество тяжелых изотопов кислорода и водорода в моче.
Дело в том, что водород может выйти из организма только с мочой (и совсем немного – с потом), а кислород – с мочой и углекислым газом. Поэтому разница в числе тяжелых изотопов водорода и кислорода равна количеству «улетевшего» углекислого газа, которое можно потом пересчитать на сожженные калории. Таким способом определяют базовые энергозатраты для каждого человека в отдельности, а потом из них вычитают нужные проценты, например в проекте CALERIE это было 20–25 %.
когда организму не хватает ресурсов, он может расходовать запасы более экономно и эффективно. Количество килокалорий, которые мы тратим на базовый обмен веществ, работу иммунитета, физическую активность и прочие статьи расходов, может изменяться в зависимости от того, сколько всего килокалорий поступает в организм. Всегда находится что-то, на чем можно сэкономить – например, перестать использовать расточительный гликолиз и перейти на кислородное дыхание.
Если уж что и ограничивать, так это потребление белков – основных источников сигнала для mTOR. Причем в экспериментах на мышах было установлено, что достаточно ограничить поступление в организм только одной аминокислоты, чтобы получить заметный эффект.
Углеводы при ближайшем рассмотрении тоже оказываются не самой полезной пищей. Ведь именно в ответ на глюкозу в крови поджелудочная железа выделяет инсулин, а клетки запускают гликолиз.
Оставшись без глюкозы, печень начинает производить ее заново. Для этого приходится обратить вспять те химические реакции, с помощью которых глюкозу обычно расщепляют. Однако до настоящей глюкозы дело не доходит, и образуются промежуточные соединения – кетоновые тела. Это короткоцепочечные жирные кислоты, которые то и дело разваливаются до ацетона – самого известного кетона, и в крови повышается концентрация кетонов. Именно поэтому диету с ограничением углеводов и преобладанием жиров называют кетогенной, а от людей, которые ее придерживаются, может пахнуть ацетоном.
Клетки других органов ловят кетоновые тела из крови и уже из них добывают энергию. Таким образом, клетки не получают глюкозы и не запускают работу mTOR. В то же время короткоцепочечные жирные кислоты подавляют воспаление и блокируют активность ферментов, которые отвечают за возрастную переупаковку ДНК.
Мода на кетогенную диету давно уже захватила Кремниевую долину, однако насколько она безопасна, до сих пор неизвестно. Можно, конечно, назначить углеводы и белки главными врагами, но как тогда быть с жирами? Пока неясно, не повышает ли кетогенная диета у человека риск атеросклероза и ожирения тканей, как это было замечено у мышей.
Третий пункт, который необходимо прописать в диете – когда нужно есть? Ограничивать калории можно самыми разными способами: можно есть постоянно только низкокалорийную пищу, а можно просто время от времени голодать, так чтобы усредненное потребление калорий оставалось ниже нормы. Существует несколько методик и такого интервального или периодического голодания: можно воздерживаться от еды по 16 часов каждый день, или через день, или 2 дня через 5 и так далее.
интервальное голодание связано с биологическими ритмами человека. Мы уже говорили о том, что поступление еды в «нерабочее» время подстегивает работу mTOR. Поэтому, возможно, полезно есть только в светлое время суток, не нарушая естественный цикл, – в этом смысле может сработать вариант «есть в течение 10–11 часов в сутки». А идеальный вариант, судя по всему, был бы синтезом двух основных: есть в течение лишь нескольких часов в сутки и при этом ограничивать калории. По крайней мере, в недавнем эксперименте на мышах такое совмещение методов дало лучший результат, чем каждый в отдельности.
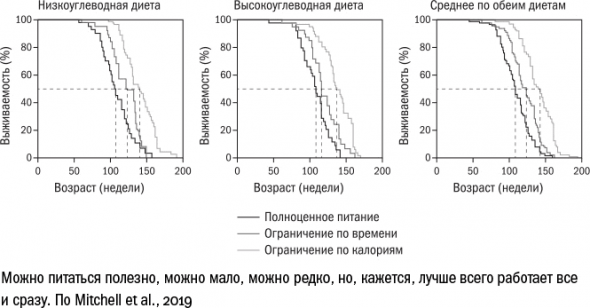
Хорошо бы найти какой-нибудь способ ограничивать в еде не человека целиком, а отдельные его клетки.
Иными словами, была бы очень кстати какая-нибудь «голодная таблетка» (по-научному – калоримиметик, имитатор ограничения калорий), которую можно принять после еды и сделать вид, что не ел. Как ни удивительно, такая таблетка действительно существует. Причем, когда ее обнаружили, оказалось, что этот препарат в медицине известен уже несколько десятков лет. Имя ему – рапамицин.
Рапамицин открыли в начале 70-х годов прошлого века, когда изучали образцы почвы с острова Пасхи. Вместе с почвой в образец попали местные бактерии, которые в лаборатории стали выделять антибиотик – его и назвали рапамицином (рапа – в честь местного названия острова, Рапануи).
ученые нашли белок, против которого работает рапамицин, и так и назвали его – «мишень рапамицина», target of rapamycin, сокращенно TOR.
Рапамицин блокирует mTOR напрямую, в обход всех сигнальных путей. Поэтому под его действием и опухоли растут медленнее, и иммунные клетки не работают, и обычные клетки приостанавливают свою энергетическую гонку и не торопятся стареть, и даже эпигенетический возраст у них не растет. В тестовых экспериментах на мышах рапамицин действительно продлил их жизнь, за что авторы проекта получили одну из премий «Мафусаилова мышь»
Аналоги рапамицина проверили в небольших концентрациях на пожилых людях, у которых за год приема препарата не возникло серьезных побочных эффектов, зато болели они реже, чем их сверстники.
Параллельно с рапамицином идут поиски и других калоримиметиков. Геронтологи наткнулись на метформин.
мыши, которых кормили метформином, прожили на треть дольше контрольных.
сейчас готовится к запуску первое его клиническое испытание на здоровых людях, TAME (targeting aging with metformin, дословно «борьба со старением с помощью метформина»). Показательно, что деньги на это исследование авторы проекта собирают через краудфандинг.
Каскад mTOR можно блокировать и на другой стадии – не до, а после активации mTOR. Так, судя по всему, работает ресвератрол – еще одно перспективное лекарство от старения. Он активирует сиртуины – белки, которые регулируют упаковку ДНК в ядре.
Кроме того, ресвератрол, как и многие вещества растительного происхождения (а он содержится, например, в кожуре винограда и орехах), обладает множеством биологических функций и в том числе может работать как антиоксидант.
Ресвератрол считается самой распространенной и безопасной биодобавкой против старения.
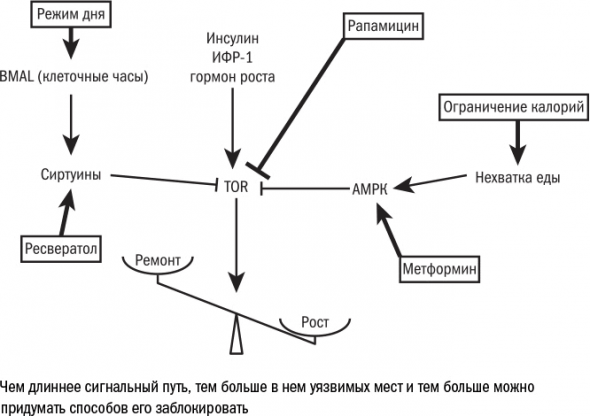
И пусть мы пока не знаем, какое из этих средств – ресвератрол, рапамицин, метформин или какой-то другой калоримиметик – поможет людям справиться с возрастными болезнями, сам факт, что есть множество способов подействовать на один и тот же механизм, позволяет надеяться, что мы на правильном пути. Так или иначе, все они работают по принципу «тише едешь – дальше будешь» и мешают комплексу mTOR гиперстимулировать клетки. Фактически они вмешиваются в программу развития и тормозят рост организма, делая его молодость – хотя бы на клеточном уровне – не такой бурной, как она могла бы быть.
Заключение
Кто виноват
процесс старения сложно свести к чему-то одному.
старение — густая сеть событий, которые происходят в организме одновременно. Старение – это и накопление мутаций, и захват ткани клонами, и рост иммунной агрессии, и разомкнутая цепь гормональной регуляции. Это деградация, в ответ на которую организм перестраивается, жертвуя одними процессами и усиливая другие. Старение – это режим, в котором организм борется со временем.
со временем организм копит микроскопические повреждения: мутации, свободные радикалы, белковые агрегаты. Клетки перестают работать и превращаются в агрессивных чужаков. Разворачивается гражданская война: иммунитет против собственных постаревших сограждан.
Каждая из теорий предсказывает свое средство продления жизни, и наиболее верной придется признать ту, чья таблетка от старости окажется самой действенной. Однако поскольку единственной причины старения, кажется, нет, то стоит смириться с тем, что никакая таблетка от старости не сможет работать в одиночку.
Обри ди Грея прав, что Борьба со старением потребует самых разных инструментов и тактик.
Ни рапамицин, ни метформин, ни сенолитики, ни антиоксиданты с горметинами – ничто из этого само по себе не способно расправиться с врагом и остановить наши внутренние часы. Лучшее, на что мы можем рассчитывать в ближайшие годы, – это получить доказательства безопасности этих средств и, возможно, добиться прогресса в борьбе с возрастными болезнями.
за последний год одна за другой начали выходить статьи, авторы которых уже пробуют новые комбинации – генов, гормонов, лекарств.
Есть основания полагать, что разные средства продления жизни способны действовать сообща.
Например, нематоды с мутацией в белке каскада TOR живут на 30 % дольше, а с мутацией в аналоге ИФР-1 – на 200 %.
Продолжительность жизни червей с обеими мутациями оказалась в пять раз выше средней.
А это означает, что если один и тот же механизм – «программу развития и молодости» – заблокировать в нескольких местах, то эти вмешательства не только дополняют, но и усиливают друг друга.
То же известно и про мышей. Самый серьезный результат по продлению жизни, который пока достигнут на млекопитающих, получили, когда морил голодом карликовых мышей. Их карликовость говорит о том, что плохо работает сигнальный каскад гормона роста, следовательно, хуже работает mTOR. А ограничение калорий тормозит его дополнительно.
На мышах испытывают генетические коктейли.
В первом же испытании «коктейля молодости» из метформина, гормона роста и ДГЭА
на человеке удалось получить первое свидетельство эпигенетического «омоложения» – по крайней мере, клеток крови.
мы уже сегодня можем представить себе, как будет устроен многокомпонентный эликсир бессмертия:
в его основе будет какое-нибудь средство, чтобы остановить квазипрограмму: рапамицин, метформин или другой блокатор mTOR-каскада, а может быть, даже не один.
Вторым слоем – станут препараты, которые целятся в непосредственные причины старения. Среди них наверняка будет активатор теломеразы, который позволит клеткам делиться дольше, и какой-нибудь препарат, способный репрограммировать клетки, то есть вернуть их ближе к стволовому состоянию. К этой же группе можно отнести и генную терапию.
Третий слой – профилактика старения. Для этого, вероятно, будут служить горметины, или уже известные, или новые, синтетические. Какой из них окажется самым эффективным: физкультура, голодание, перепады температуры или токсины, – нам еще предстоит выяснить.
Наконец, с некоторыми признаками старения придется бороться постфактум – это тот самый ремонт, на котором призывает сосредоточиться Обри ди Грей. Здесь в качестве четвертого слоя нам понадобятся сенолитики для очистки тела от старых клеток и, возможно, какие-нибудь другие препараты, например, чтобы расщеплять сшивки в молекулах межклеточного вещества или растворять белковые агрегаты в тканях.
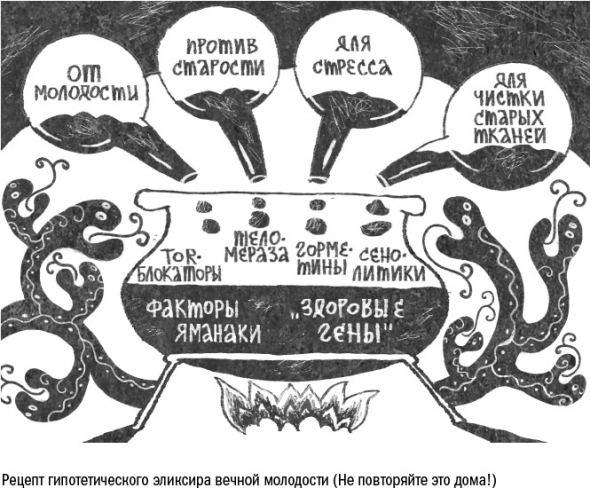
Пока от эликсира нас отделяет долгая дорога, полная испытаний.
теги блога Андрей Колесников
- Amazon
- ChatGPT
- ETF
- ICO
- netflix
- telegram
- акции
- банки
- баффет
- безработица
- Биохакинг
- биткоин
- блокчейн
- видеоКонспект
- газпром
- геополитика
- геронтология
- демография
- долголетие
- Доллар рубль
- здоровый образ жизни
- здоровье
- ЗнанияСжато
- ЗОЖ
- золото
- ИИ
- Илон Маск
- инвестирование
- инвестиции
- Инновации
- инфляция
- искусственный интеллект
- история
- история России
- Китай
- коронавирус
- короновирус
- Красная Таблетка-2
- кризис
- кризис 2020
- кризис2020
- криптовалюта
- магия утра
- ментальные ловушки
- меры поддержки бизнеса
- мировая экономика
- мобильный пост
- Мовчан
- мозг
- Мошенничество
- мышление
- нейробиология
- Нефть
- Облигации
- олигархи
- опек+
- опрос
- оффтоп
- пандемия
- Пелевин
- поведенческая экономика
- подсознание
- предпринемательство
- предпринимательство
- психология
- Путин
- ресурсное "проклятие"
- Рэй Далио
- самодисциплина
- саморазвитие
- санкции
- сбербанк
- СВО
- Собянин
- стартапы
- счастье
- сша
- тайм-менеджмент
- ТГ-канал kudaidem
- ТГ-канал SmartEventMos
- технологии
- Трамп
- трейдинг
- Утро
- финам
- форекс
- ФРС
- футурология
- цифровизация
- экономика
- экономика Китая
- экономика России
- экономика США
- экономическая история
- эмиграция
- Энергетический кризис
- эффективность
- Яндекс




















95% потребителей красивых биодобавок потребляют недостаточное количество аминокислот… их тела и мозги подобны стройкам, на которые поставляется мало стройматериалов… поэтому они успешно стареют, болеют и тупеют… обложившись баночками с приятными названиями))
мы — белковая форма жизни… поэтому, для нашего здоровья нужны в достаточном количестве (в порядке убывания важности):
1. аминокислоты (в простонародье — белки)
2. микроэлементы
3. витамины
За надлежащим количеством этих компонент в питании нужно следить так же внимательно, как за октановым числом бензина, заливаемого в бак личного авто))
Это и есть аминокислота.
как ужин врагу)
Штэ? ))
Много буков но плюсанул — тема интересная, но старая.
Рецепт молодости изобрёл ещё Станислав Лем в 1960х
В тело вводятся нанороботы, которые устраняют проблемы и латают клеточные мехонизмы. Что нельзя залатать — заменяется искуственными молекулярными дубликатами.
Через несколько сотен лет человек представлял бы собой полностью бессмертную синтетическую конструкцию по образу и подобию.
----
В общем идея в том что никаким физическим законам «вечное омоложение» не противоречит, нужен просто соотв. алгоритм и приток энергии.
Это как холодильник не противоречит физике, хотя в окружающем мире мы видим что холодное нагревается, горячее — остывает, а в холодильнике этот процесс идёт вспять ))